Akzeptanz von künstlichem Nektar als Ersatzfutter für Schmetterling am Beispiel von zwei Heliconius-Arten
Zusammenfassung
Bei der Bereitstellung von ausreichend Nektarpflanzen bei der Zucht von Schmetterlingen können z.B. jahreszeitlich bedingt Engpässe entstehen. Daher ist es wünschenswert, künstlichen Nektar als Ersatz vorzuhalten. Die Akzeptanz von künstlichen Nektarmischungen ist nicht bekannt.
In einem künstlichen Habitat nach dem Prinzip eines „Living Tropical Greenhouses“ wurde Kolonien von neotropischen Heliconius erato bzw. Heliconius melpomene standadisiert zwei künstliche Nektarlösungen (reine Fruktose vs. neuer Kunstnektar mit unkl. Zusammensetzung) angeboten und die Akzeptanz an künstlichen Blüten gemessen.
Die Nahrungsaufnahme der beobachteten Schmetterlingsarten unterliegt tageszeitlichen Schwankungen. Die Schwankungen können als Folge eines engumschrieben Temperaturoptimums interpretiert werden. Beide künstlichen Nektarlösungen wurden prinzipiell akzeptiert. Im zeitlichen Verlauf wurde reine Fruktose-Lösung jedoch signifikant bevorzugt (Fruktose-Lösung n = 169, 64 vs. neuer Kunstnektar n = 94, 36%, p < 0.001). Es können keine Aussagen zu möglichen positiven oder negativen Auswirkungen des neuen Kunstnektars auf Vitalität oder Fertilität gemacht werden. Der Beobachtungsezitraum war hierfür zu kurz im Verhältnis zur Langlebigkeit der beobachteten Schmetterlinge.
Der neue Kunstnektar wird prinzipiell als Ergänzungsnahrung angenommen, reine Fruktose-Lösung jedoch bevorzugt. Möglicherweise läßt sich die Akzptanz des neuen Kunstnektar durch Beimischung von Fruktose verbessern. Wünschenswert wäre für Heliconius-Schmetterlinge eine Ergänzung durch Aminosäuren.
Hintergrund
Nicht nur unter wissenschaftlichen Gesichtspunkten ist die Haltung und Zucht von einheimischen und exotischen Schmetterlingen verbreitet, auch eine große Zahl von Hobbiisten widmet sich diesem Thema. Die Versorgung der adulten Schmetterlinge mit ausreichend Nektar kann in klimatisch schwierigen Zeiten (Vorfrühling, Herbst / Winter) oder bei plötzlichem Schlupf einer großen Anzahl von Schmetterlingen ein Problem darstellen. Es ist daher wünschenswert, eine einfach zu bevorratende Ersatz- oder Ergänzungsnahrung vorzuhalten. Hier soll ein neuentwickelter künstlicher Nektar auf die Akzeptanz untersucht und mit einer einfachen Fruktuosemischung verglichen werden.
Testumgebung
Als Testumgebung dient ein isoliertes Gewächshaus 2.5 x 4 Meter. Da der künstliche Nektar an tropischen Schmetterlingen getestet werden soll, werden ensprechende klimatische Bedingungen geschaffen. Die Temperatur liegt tagsüber um 27°C, nachts um 15°C. Zu beachten ist jedoch ein vertikaler Temperaturgradient. Zur Mittagszeit können unter dem Glasdach bis 40°C herrschen, während am Boden um 22°C vorliegen. Die Luftfeuchtigkeit schwankt um 80% RH. Eine ausführliche Beschreibung findet sich an anderer Stelle. (Siehe Tropenhaus)

Grafik 1 - Tropenhaus
Testpopulationen
Als Testpopulationen dienen eine reproduktiv stabile Kolonie Heliconius erato petiverana (Ursprungsland Costa Rica), sowie einige Subspecies-Hybriden mit ca. 20 adulten Schmetterlingen, sowie eine labile Kolonie Heliconius melpomene, bestehen aus 10 Hybriden in mehrfacher Tochtergeneration. Weiterhin sind Eier, Raupen und Puppen in unbestimmter Anzahl in der Testumgebung vorhanden. Die Kolonien werden nach dem Prinzip des „Living Tropical Greenhouse“ gehalten (Tampion & Tampion 1999). Darunter verstehen wir eine kontinuierlich Generationsfolge in einem weitgehend abgeschlossenen künstlichen Lebensraum. Raupenfutterpflanzen und Nahrungspflanzen für adulte Schmetterlinge befinden sich innerhalb dieses künstlichen Lebensraumes und werden möglichst wenig von außen ergänzt. Die Schmetterlinge haben daher bei Testbeginn ein sehr unterschiedliches Alter (0 bis 150 Tage).

Grafik 2 – Heliconius erato petiverana

Grafik 3 – Heliconius melpomene-Hybrid
Natürliche Ernähung der adulten Schmetterlinge
Ein Teil der Ernährung dieser Schmetterlingsarten im natürlichen Habitat besteht aus Nektar. Dort werden u.a. Lantana camara aufgesucht. Heliconius-Schmetterlinge nehmen eine Reihe von volatilen Bestandteilen von Blühpflanzen war. (Andersson & Dobson 2003b) Frisch geschlüpfte Falter finden Nektarreiche Pflanzen zunächst anhand des Geruchssinns, später anhand der Blütenfarbe. Die Schmetterlinge sind lernfährig. So wird später eine Assoziation zu gelber Blütenfarbe hergestellt. (Andersson & Dobson 2003a) Weiterhin ergänzen die beiden untersuchten Heliconius-Arten ihre Nahrung durch Pollen. H. melpolme sucht ganz überwiegend Pollen von Curbitacaea (Psiguria und Gurania). H. erato vermag auch Pollen von z.B. Lantana camara zu utilisieren. (Estrada 2002)Der Mundapparat der Schmetterlinge sind entsprechend angepasst. (Krenn & Penz 1998; Eberhard et al 2009) Dabei verfügen Heliconius-Schmetterlinge über ein sehr gutes Ortsgedächtnis und suchen Pollenlieferanten regelmäßig wieder auf. H. erato kann auch Pollen von Lantana sp. verwenden. (Estrada 2002)
Ernährung im künstlichen Habitat
Die Testpopulationen werden als Grundnahrung mit Nektar verschiedener Blühpflanzen versorgt (Siehe Tabelle 1). Dabei steht Lantana und Pentas ganz im Vordergrund.
|
Spezies |
Anzahl der Pflanzen |
Anzahl der Blütenstände (Tages-Durchschnitt) |
Höhe der Blütenstände (cm) vom Boden gemessen |
|
Lantana camara |
5 |
15 |
50 - 250 |
|
Pentas lanceolata |
17 |
55 |
20 – 120 |
|
Verbena spp. |
4 |
4 |
30 – 200 (1) |
|
Buddleia sp. |
1 |
2 |
120 – 150 |
|
Cestrum spp. |
3 |
3 |
30 – 150 |
|
Passiflora spp. |
50 |
15 |
30 – 250 (2) |
Tabelle 1: vorhandenen Nektarpflanzen im Gewächshaus. (1) Zwei Verbenen werden als Hänge-pflanzen kultiviert. (2) Passiflora wird nur selten als Nektarlieferant genutzt.

Grafik 4 – Nektarpflanzen im Tropenhaus
Die Pollenlieferanten Psiguria oder Gurania sind leider in Deutschland nicht erhältlich. Versuche mit anderen Curbitacaea sind nicht erfolgreich verlaufen. Auf Kunstblüten angebotener Pollen wurde nicht akzeptiert. Einige der Schmetterlige haben jedoch gerlernt, aus verwelkten Passionsblumen-Blüten Pollen zu gewinnen. Dies wird an anderem Ort berichtet.
Weiterhin wurde bereits vor Testbeginn eine einfache Fruktose-Mischung (20%) als Ergänzungsnahrung angeboten. Die Schmetterlinge hatten also bereits das Prinzip der künstlichen Blüte erlernt. (Grafik 5)

Grafik 5 – Schmetterlinge auf künstlicher Blüte vor Testbeginn.
Versuchsaufbau
Es werden nach einander drei Versuche durchgeführt. Zunächst soll getestet werden, ob prinzipiell die Fruktosemischung und der Kunstnektar akzeptiert werden. In einem zweiten Versuch soll geprüft werden, ob die unterschiedlichen Kunstfutter evtl. mit dem Geruchssinn erkannt werden können. Im dritten Versuch wird die Präferenz der Schmetterlinge getestet.
Vorbereitung der Nektarlösungen
Als Vergleichsnektar dient eine 20%-ige Fruchtzucker-Mischung. Diese Zuckerlösung wurde vor Versuchsbeginn schon als Zustatznahrung angeboten. Diese Lösung wird mit A bezeichnet.
Der neue Kunstnektar wurde zur Verfügung gestellt als weißes Pulver (180 g). Die genaue Zusammensetzung ist uns nicht bekannt. Enthalten sein sollen Zucker, Mineralien und Vitamine. („Das Präparat besteht vorwiegend aus verschiedenen Zuckern, die mit einigen Spuren von Mineralien und Vitaminen versetzt sind.“) Das Pulver schmeckt süß. Nach Anweisung der Entwickler soll der neue Kunstnektar in 100 ml stillem Mineralwasser gelöst werden. Da eine solch große Menge nicht verbraucht werden kann, werden Portionen zu je 10 ml hergestellt. Eine Feinwaage steht nicht zur Verfügung, daher wird eine 20%-Lösung (Volumenprozent) als genauest mögliche Mischung angefertigt. Diese Lösung wird mit B bezeichnet.
Reste der Lösungen werden im Gewächshaus gelagert.
Grafik 6 – Vorbereitete Testlösungen: A – reine Fruktose-Lösungs, B – neuer Kunstnektar
Versuch 1 – Test of priciple
Schmetterlinge werden in ihrem natürlichen Verhalten beobachtet. Sobald sie an einem Lantana- oder Pentas-Blütenstand Nektar saugen, wird ihnen in bzw. direkt neben dem Blütenstand eine Spritze mit eine der beiden Lösungen angeboten. Sobald der Rüssel zufällig in die Spritze gelangt, wird registriert, ob der Schmetterling Nahrung aufnimmt. Verbleibt der Rüssel länger als zwei Sekunden in der Spritze, wird dies als Nahrungsaufnahme gewertet.

Grafik 7 – Versuch 1: Innerhalb eines Blütenstandes wird Testlösung angeboten

Grafik 8 – Versuch 1: Schmetterling nimmt Nahrung aus einer Spritze auf.
Versuch 2 – Testung des Geruchs
Schon vor Versuchsbeginn wurden den Schmetterlingen eine Fruktose-Lösung als Zusatznahrung angeboten. Als künstliche Blüte dienen hierzu ein Reservoir (7.5 ml) und ein Filzquadrat (7.5 x 7.5 cm). Der Filz nimmt ca. 8 ml Feuchtigkeit auf, bis er durchfeuchtet ist. Darunter verstehen wir, so nass, dass gerade kein Tropfen herunterfällt. Für die Versuche 2 und 3 werden solche künstliche Blüten verwendet. Um gleiche Bedingungen für einen Vergleich der Testlösungen zu gewährleisten, werden zwei identische künstliche Blüten in gleicher Höhe (ca. 160 cm vom Boden) nebeneinander aufgehängt. Die künstlichen Blüten liegen im Halbschatten, um eine Verdunstung zu minimieren. Weiterhin liegen die künstlichen Blüten außerhalb der Reichweite von Nebeldüsen, damit es zu keiner Verdünnung kommt und um zu verhindern, dass eine bloße Feuchtigkeitsaufnahme fälschlicherweise als Nahrungsaufnahme gewertet wird.

Grafik 9 – Künstliche Blüten: Der Schmetterling nimmt Nektar direkt aus dem Vorrat auf, was selten der Fall ist.
Im Versuch 2 wird zunächst nur das Reservoir mit der jeweiligen Testlösung befüllt, um zu beobachten, ob möglicherweise durch Geruch Schmetterlinge angelockt werden. Besuche die länger als zwei Sekunden dauern, werden als Versuch der Nahrungsaufnahme gewertet.
Versuch 3 – Vergleich der Präferenz
Der dritte Versuch untersucht die Präferenz der Schmetterlinge. Besuche der künstlichen Blüten, die länger als zwei Sekunden dauern, und bei denen es offensichtlich zum Saugen kommt, werden als Nahrungsaufnahme gewertet. Eine Untersuchungszeiteinheit beträgt 10 Minuten. An einer Reihe aufeinanderfolgender Tage werden zu multiplen Tageszeiten die Anzahl der Blütenbesuche zur Nahrungsaufnahme registriert. Zeit und klimatische Bedingungen werden dokumentiert.

Grafik 10 – Anordnung der künstlichen Blüten

Grafik 11 – Typische Beobachtungssituation: Lantana camara wird deutlich bevorzugt. Beide Kunstbüten werden angeflogen. Film 1 - Typische Beobachtungssituation
Statistische Auswertung
Die Ergebnisse werden mithilfe eines Chi-Quadrat-Tests ausgewertet. Das prädefinierte Signifikanzniveau beträgt p < 0.05. Weiterhin wird das relative Verhältnis der Blütenbesuche zur Nahrungsaufnahme der Temperatur und dem Zeitverlauf gegenübergestellt und mittels Regressionsanalysen mögliche Korrellationen untersucht.
Ergebnisse
An insgesamt 11 aufeinander folgenden Tagen wurde die Anzahl der Blütenbesuche zur Nahrungsaufnahme registriert. Die Ergebnisse sind nachfolgend zusammengestellt.
Versuch 1
An drei Beobachtungsintervallen werden, wie oben beschrieben, die zwei unterschiedlichen Kunstnektarmischungen in einer Spritze angeboten. In der Mehrzahl der Fälle wird kein Kunsstnektar angenommen, sondern der natürliche Blütenstand bevorzugt.
|
Tag |
Uhrzeit |
A |
A + B |
B |
0 |
Temperatur |
Wetter |
|
Sa |
11:00 |
2 |
1 |
1 |
2 |
27 |
sonnig |
|
Sa |
13:00 |
2 |
0 |
3 |
7 |
27 |
sonnig |
|
Sa |
14:00 |
1 |
0 |
0 |
6 |
28 |
sonnig |
|
Summe |
|
5 |
1 |
4 |
15 |
|
|
Tabelle 2: prinzipielle Akzeptanz der Kunstnektarlösungen, A = Fruktose, B = Kunstnektar
In einer Auswertung dieser orientierenden Untersuchung besteht kein signifikanter Unterschied zwischen den beiden Kunstnektarlösungen (A = 5 vs. B = 4, nicht signifikant).
Versuch 2
An einem Vormittag werden beide Kunstnektarlösungen nur über ein Röhrchen-Reservoir angeboten. Hiermit soll eine mögliche Bevorzugung durch eine Geruchskomponente untersucht werden. An zwei Beobachtungsintervallen werden Besuche auf der Kunstblüte gezählt. Ein nennenswerter Anflug der künstlichen Blüten fand nicht statt.
|
Tag |
Uhrzeit |
A |
B |
Temperatur |
Wetter |
|
Sa |
10:00 |
0 |
1 |
26 |
sonnig |
|
Sa |
11:00 |
0 |
0 |
27 |
sonnig |
|
Summe |
|
0 |
1 |
|
|
Tabelle 3: Untersuchung einer möglichen Geruchskomponente, A = Fruktose, B = Kunstnektar
Die Zahl der Beobachtungsintervalle ist zu klein, um eine statistische Auswertung zu ermöglichen.
Versuch 3
Im Hauptversuch der Untersuchung wird untersucht, wie oft Schmetteringe die Kunstblüten zur Nahrungsaufnahme aufsuchen. Mehrfach täglich werden die Kunstnektarlösungen nachgefüllt, so dass das Reservoir stets gefüllt und das Vlies immer tropfnass ist. An 11 aufeinanderfolgenden Tagen zu multiplen Beobachtungsintervallen erfasst, wie oft die beiden Kunstnektarlösungen aufgenommen werden. Beobatchtungszeitpunkt, Temperatur und Wetter (Sonneneinstrahlung) werden dokumentiert. Insgesamt werden an 43 Beobachtungsintervallen insgesamt 263 Besuche der Kunstblüten mit Nahrungsaufnahme (Saugen länger als zwei Sekunden) beobachtet.
|
Tag |
Uhrzeit |
Fruktose |
Kunstnektar |
Temperatur |
Wetter |
|
Sa |
11:00 |
0 |
1 |
25 |
sonnig |
|
Sa |
12:00 |
0 |
0 |
27 |
sonnig |
|
Sa |
13:00 |
2 |
3 |
28 |
sonnig |
|
Sa |
14:00 |
2 |
3 |
30 |
sonnig |
|
Sa |
15:30 |
2 |
2 |
27 |
bedeckt |
|
So |
08:30 |
7 |
4 |
19 |
sonnig |
|
So |
09:30 |
9 |
7 |
23 |
sonnig |
|
So |
10:30 |
3 |
20 |
25 |
sonnig |
|
So |
13:00 |
2 |
5 |
28 |
sonnig |
|
So |
14:30 |
4 |
2 |
29 |
sonnig |
|
So |
15:30 |
5 |
4 |
29 |
sonnig |
|
So |
16:30 |
0 |
0 |
28 |
sonnig |
|
Mo |
12:00 |
0 |
3 |
28 |
sonnig |
|
Mo |
16:30 |
3 |
4 |
28 |
sonnig |
|
Mo |
17:30 |
0 |
2 |
26 |
bedeckt |
|
Di |
14:00 |
1 |
3 |
29 |
sonnig |
|
Di |
16:30 |
5 |
7 |
26 |
sonnig |
|
Mi |
16:30 |
6 |
4 |
26 |
sonnig |
|
Mi |
17:30 |
1 |
0 |
26 |
sonnig |
|
Do |
16:30 |
4 |
1 |
27 |
sonnig |
|
Do |
17:30 |
2 |
1 |
27 |
sonnig |
|
Fr |
13:00 |
1 |
0 |
30 |
sonnig |
|
Fr |
15:00 |
2 |
2 |
30 |
sonnig |
|
Fr |
16:30 |
2 |
0 |
28 |
sonnig |
|
Fr |
17:30 |
0 |
0 |
27 |
sonnig |
|
Sa |
09:30 |
19 |
4 |
23 |
sonnig |
|
Sa |
10:30 |
15 |
1 |
25 |
sonnig |
|
Sa |
12:30 |
1 |
1 |
29 |
sonnig |
|
Sa |
13:30 |
7 |
0 |
28 |
sonnig |
|
Sa |
15:30 |
3 |
1 |
29 |
sonnig |
|
Sa |
16:30 |
2 |
0 |
29 |
sonnig |
|
So |
08:30 |
2 |
0 |
19 |
sonnig |
|
So |
10:00 |
7 |
1 |
23 |
sonnig |
|
So |
11:00 |
8 |
0 |
25 |
sonnig |
|
So |
16:30 |
2 |
1 |
27 |
sonnig |
|
Mo |
09:00 |
11 |
1 |
23 |
sonnig |
|
Mo |
10:00 |
3 |
1 |
25 |
bedeckt |
|
Mo |
11:00 |
5 |
1 |
25 |
bedeckt |
|
Mo |
12:00 |
7 |
1 |
25 |
bedeckt |
|
Mo |
13:00 |
5 |
1 |
26 |
bedeckt |
|
Mo |
14:30 |
3 |
0 |
26 |
bedeckt |
|
Mo |
15:30 |
0 |
0 |
26 |
bedeckt |
|
Mo |
17:00 |
0 |
0 |
25 |
bedeckt |
|
Summe |
|
169 |
94 |
|
|
Tabelle 4: Versuch 3 – Anzahl der Blütenbesuche zur Nahrungsaufnahme
Zunächst werden die Habitatbedingungen analysiert. Es bestand eine stabile Schönwetterlage. Zehn Tage Sonnenschein Ende September sind sehr ungewöhnlich. Die gleichbleibende Wetterlage erleichtert eine Interpretation der Untersuchungsergebnisse.
Die Tempertur wird in 1.0 Metern Höhe im Schatten gemessen. Die nächtlichen Temperaturen liegen (bei laufender Heizung) bei 15°C. Ab 8:00 Uhr wird die Temperatur durch Heizung und Sonneneinstrahlung erhöht. Gegen 13:00 Uhr wird ein Maximum um 29°C erreicht. Ab ca. 16:30 Uhr fällt die Temperatur wieder unter 28°C.
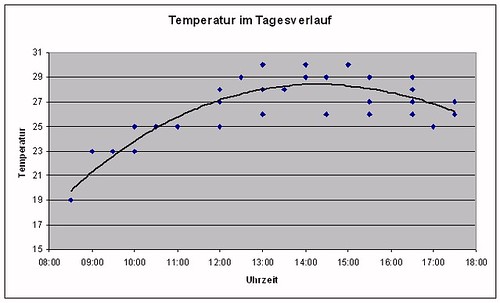
Grafik 12 – Temperatur im Tagesverlauf
Die Aktivität und damit auch die Nahrungsaufnahme der Schmetterlinge schwanken im Tagesverlauf. Das Verhaltensrepertoir der Schmetterlinge soll später umfassend quantitativ untersucht und an anderem Ort beschrieben werden. Hier wird lediglich die Nahrungsaufnahme beschrieben.
Insbesondere morgens werden häufig Blütenbesuche beobachtet. Um die Mittagszeit werden Blütenbesuche seltener um dann in den Nachmittagsstunden wieder häufiger beobachtet zu werden.
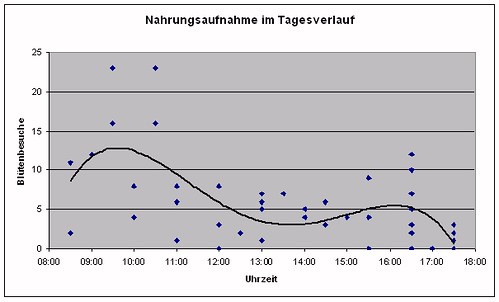
Grafik 13 – Nahrungsaufnahme im Tagesverlauf
Stellt man die beiden Testlösungen einander gegenüber, so ergibt sich eine im Tagesrhythmus entsprechende Frequentierung.
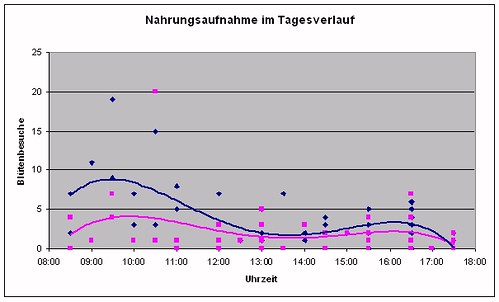
Grafik 14 – Nahrungsaufnahme im Tagesverlauf, blau: Fruktose-Lösung, rosa: neuer Kunstnektar
Untersucht man den Einfluss der Temperatur auf die Nahrungsaufnahme, so wird deutlich, dass die größte Aktivität zwischen 23 und 25°C beobachtet werden kann.
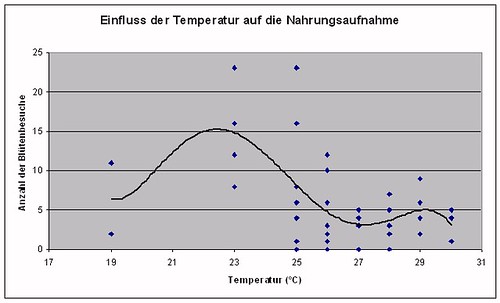
Grafik 15 – Einfluss der Temperatur auf die Nahrungsaufnahme
Hierbei ist die Temperaturtoleranz von Heliconius erato offenbar größer als die von Heliconius melpomene. (Hier nicht dokumentiert.) Heliconius melpomene wird erst ab 25°C aktiv. Heliconius erato wurde schon bei deutlich niedrigeren Temperturen bei Blütenbesuchen beobachtet. Oberhalb von 29°C nimmt die Aktivität wieder ab. Bei diesen Temperaturen suchen die Schmetterlinge kühlere Bereiche in Bodennähe auf. Zum Teil werden dort die heißen Mittagsstunden in Inaktivität verbracht.
(Wird noch eingestellt.)
Grafik 16 – Schmetterling inaktiv in Bodennähe (13:30 Uhr, Temperatur in 1.0 Meter im Schatten 29°C)
Es werden die Anzahl der Blütenbesuche mit Nahrungsaufnahme (Saugen länger als zwei Sekunden) registriet und gegenübergestellt. Es besteht insgesamt eine signifikante Präferenz für reine Fruktose-Lösung, (Fruktose-Lösung n = 169, 64 vs. neuer Kunstnektar n = 94, 36%, p < 0.001).
Die Anzahl der Blütenbesuche wird im Folgenden zeitlich nach Tagen aufgeschlüsselt.
|
Wochentag |
Fruktose-Lösung |
Neuer Kunstnektar |
|
Sa |
8 |
10 |
|
So |
29 |
43 |
|
Mo |
3 |
9 |
|
Di |
6 |
10 |
|
Mi |
7 |
4 |
|
Do |
6 |
2 |
|
Fr |
5 |
2 |
|
Sa |
47 |
7 |
|
So |
19 |
2 |
|
Mo |
39 |
5 |
|
Summe |
169 |
94 |
Tabelle 5: Versuch 3 – Zeitliche Aufschlüsselung der Blütenbesuche
Vergleicht man die relative Häufigkeit der Blütenbesuche an den ersten beiden Beobachtungstagen und an den beiden letzten Boebachtungstagen, so erkannt man ein hochsignifikate Änderung des Verhaltens. Während an den ersten beiden Tagen der neue Kunstnektar noch bevorzugt wird (59% vs. 41%, p < 0.01), so überwiegt an den letzten beiden Beobachtungstagen die Nahrungsaufnahme von Fruktose-Lösung (89% vs. 11%, p < 0.0001).
Auch bei einer graphischen Regressionsanalyse wird deutlich, dass anfangs beide Kunstnektarlösungen in etwa gleich beliebt sind. Zum Ende der Untersuchung überwiegt die Fruktose-Lösung deutlich.
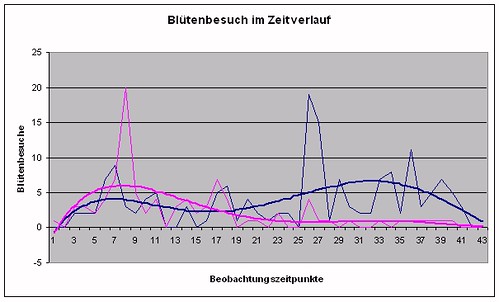
Grafik 17 – Blütenbesuche im Zeitverlauf, blau: Fruktose-Lösung, rosa: neuer Kunstnektar
Diskussion
Wir konnten zeigen, dass im Tagesverlauf die Nahrungsaufnahme schwankt mit einem Gipfel am Morgen und einem zweiten Höhepunkt am Nachmittag. Diese Schwankung lässt sich gut mit Temperaturschwankungen erklären. Bei 23 bis 25°C war die Frequenz der Blütenbesuche am höchsten.
Zu Beginn der Untersuchung bestand eine geringe Bevorzugung des neuen Kunstnektars. Mit zunehmender Untersuchungsdauer wurden fast ausschließlich Blütenbesuche bei der reinen Fruktose-Lösung beobachtet.
Es ist bekannt, dass Heliconius-Schmetteringe lernfähig sind und über ein sehr gutes Ortsgedächtnis verfügen (Turner 1981). Im natürlichen Lebensraum suchen diese Schmetterlingsarten zunächst nach Geruchsreizen nach Nektarpflanzen. Später lernen sie, gelbe Blüten (z.B. Lantana camara) visuell zu erkennen. (Andersson & Dobson 2003b) Heliconius-Schmetterlinge sind ganz überwiegend ortsständig in einem Revier von ca. 1 qkm. (Turner 1981) Sie ergänzen ihre Ernährung durch Pollen, der von einigen wenigen Planzenarten, meist Kürbisgewächsen, zur Verfügung steht. Diese werden im Tagesverlauf regelmäßig wieder aufgesucht. (Estrada 2002)
Es ist daher schlüssig, dass die hier dargestellte Bevorzugung der Kunstblüten mit Fruktose-Lösung gerlernt wurde und die entsprechende Kunstblüte gezielt aufgesucht wurde.
Die genaue Zusammensetzung des neuen Kunstnektars ist mir nicht bekannt. Vom menschlichen Geschmackseindruck ist er etwas weniger süß als Fruktose. Es besteht daher die Möglichkeit, dass ein anderer Zucker hier Verwendung fand, der auch von den Schmetterlingen als weniger süß und daher weniger attraktiv wahrgenommen wird.
Man könnte zwar postulieren, dass die Schmetterling den ernährungsreleanten Nutzen selbst beurteilen könnten. Dies bleibt aber Spekulation. Um einen positiven Effekt auf die Vitalität bzw. Langlebigkeit und die Fertilität zu sehen, war der Beobachtunsgzeitraum bei diesen langlebigen Arten zu kurz. Man kann jedoch festhalten, dass durch etwa einhundert-maliger Aufnahme des neuen Kunstnektar keine direkten negativen Auswirkungen sichtbar wurden.
Interpretation
Der neue Kunstnektar wird zwar von Schmetterlingen akzeptiert. Er zeigt aber gegenüber reiner Fruktose-Lösung in der Akzeptanz deutlich Nachteile. Dies könnte evtl. durch eine Modifikation des Zuckeranteils korrigiert werden. Bezüglich der Auswirkungen auf Vitalität und Fertilität kann aufgrund des Untersuchungsaufbaus keine Aussage gemacht werden. Insbesondere für die untersuchten Schmetterlingsarten wäre eine Beigabe von Aminosäuren zu einem Kunstnektar wünschenwert. Auf Weiterentwicklungen bin ich schon gespannt.
Literatur
Andersson S, Dobson HEM, Behavioral forgaging responses by the butterfly Heliconius melpomene to Lantana camara floral scent. J Chem Ecology, Vol. 29, No. 10, 2003: 2303-2318.
Andersson S, Dobson HEM. Antennal responses to flora scents in the butterfly Heliconius melpomene. J Chem Ecology (2003), Vol 29. No. 10: 2319-2330.
Eberhard, SH, Nemeschkal, HL and Krenn, HW (2009), Biometrical evidence for adaptations of the salivary glands to pollen feeding in Heliconius butterflies (Lepidoptera: Nymphalidae). Biological Journal of the Linnean Society, 97: 604–612.
http://onlinelibrary.wiley.com/doi/10.1111/j.1095-8312.2009.01243.x/abstract
Estrada C, Jiggins CD. Pattern of pollen feeding and habitat preference among Heliconius species. Ecological Entomology (2002) 27, 448-456.
http://heliconius.zoo.cam.ac.uk/publications/Estrada2002.pdf
Krenn HW, Penz CM. Mouthparts of Heliconius butterflies (Lepidoptera: Nymphalidae): a search for anatomical adaption to pollen feeding behavior. Intl. J Insect Morph Embry, Vol 27, 4 (1998): 301-309.
Tampion & Tampion , The Living Tropical Greenhouse. 1999. Guild of Master Craftsman Publicaton Ltd, Lewes.
Turner J. R. G. 1981. Adaptation and evolution in Heliconius: a defense of NeoDarwinism. Ann. Rev. Ecol. Syst., 12: 99-121.
Dr. Holger Klee, 9 / 2011.